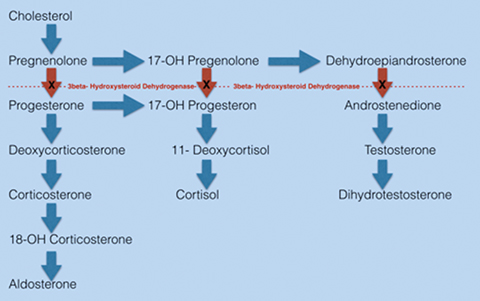
3β-Hydroxysteroid-Dehydrogenasen (3β-HSD) sind Enzyme, die in Steroiden die 3β-Hydroxygruppe zum Keton oxidieren und gleichzeitig die Umlagerung der Doppelbindung von der 5- in die 4-Position katalysieren. Diese Reaktion wird in Wirbeltieren bei der Biosynthese von Progesteron aus Pregnenolon benötigt, genauso wie bei der Umwandlung von Dehydroepiandrosteron zu Androstendion oder von 17α-Hydroxypregnenolon zu 17α-Hydroxyprogesteron.
3β-HSD sind Transmembranproteine und lokalisieren zum endoplasmatischen Retikulum und zu den Mitochondrien. Beim Menschen sind drei paraloge Isoformen bekannt, die in unterschiedlichen Gewebetypen exprimiert werden: 3β-HSD I hauptsächlich in den Brustdrüsen, der Plazenta und der Haut; 3β-HSD II vor allem in Nebennieren, Hoden und Eierstöcken. Mutationen im HSD3B2-Gen sind verantwortlich für ein adrenogenitales Syndrom Typ 2 (CAH durch 3-beta-Hydroxysteroid-Dehydrogenase-Mangel). Das dritte menschliche Enzym dieser Proteinfamilie ist 3β-HSD Typ 7, ein Enzym der Gallensäurebildung aus Cholesterin.
Katalysierte Reaktionen
NAD ⇔⇔ NADH/H
Pregnenolon wird zu Progesteron umgesetzt. Es findet nacheinander eine Dehydrierung zum Keton und eine Umlagerung der Doppelbindung statt. Eine weitere Reaktion ist die Umsetzung von DHEA zu Androstendion.
Strukturverweis
Strukturmodell von HSD3B1: siehe vierter Weblink; aus
Weblinks
- Jassal / reactome: Pregnenolone is dehydrogenated to form pregn-5-ene-3,20-dione
- Jassal / reactome: Pregn-5-ene-3,20-dione isomerizes to progesterone
- Jassal / reactome: DHA isomerizes to 4-Androstene3,17-dione
- Strukturverweis
Einzelnachweise